首先要知道體內的酸分為兩種:volatie and nonvolatile acid
1. Volatile: CO2 from the aerobic metabolism of cells
2. Nonvolatile: also called fixed acid
Includes sulfuric acid =H2SO4( product of protein catabolism) and phosphoric acid=H3PO4(phospholipid catabilism), 40-60mmole/day.
Others fixed acids 可以因為疾病如酮酸中毒也可因為攝食入如吃過多水楊酸。
接下來該知道身體有所謂的Buffer system:
相信高中都學過簡單的酸鹼滴定和緩衝溶液的計算,人體也不例外,利用緩衝溶液的弱酸弱鹼才可構成一個較不易改變的酸鹼環境。
在pK+or -1是緩衝的最好狀態。
細胞外最主要的緩衝配對離子為HCO3/CO2 and H2O(pK of the CO2/HCO3- buffer pair is 6.1) 這也是待會Anion gap中的主角。
以及Phosphate(H2PO4-/HPO4-2) buffer pair is 6.8.其中phophate在尿中的緩衝溶液又佔有非常重要的角色!
藉由排出H2PO4-來排出H+, 因此H2PO4-又稱為titratable acid.
接下來是細胞內的buffer:
- Organic phosphate(ex.AMP,ADP,ATP,2,3-DPG)
- Proteins(Hemoglobin is a major intracellular buffer.)
在正常的生理PH範圍時 deoxyhemoglobin is a better buffer than oxyhemoglobin.
接著就是一個可以由HA=H+A導出的有名公式: pH=pK+log<A->/<HA>
這個公式告訴我們如果A-=HA 時,pH=pK也就是在弱酸弱鹼對等的比例下這時溶液的緩衝效果最好。
接下來進入腎臟的酸鹼調控:
- Reabsorption of filtered HCO3-:主要發生在近曲小管
主要應該要以下這張圖來表達

可以看到CO2+H2O在近曲小管的細胞內藉由有名的enzyme (CA:carbonic anhydrase)而產生H+ and HCO3-
而此時H+藉由Na+-H+exchange in the luminal membrane而排出,但同時HCO3-卻是吸收到血液中,
而濾出的H+到lumen端和腎絲球濾過的HCO3-再度藉由brush border上的CA產生CO2+H2O而擴散入細胞再度從來循換,注意到了嗎!
整個過程H+只在循環使用,但卻造成靜吸收一個filter的HCO3-!
而其中這個吸收會受到幾個因素的調控:
- Filter load:增加filter過的HCO3-會導致增加HCO3-的吸收。
- 但是如果filter load超過吸收的capacity剩下多餘的HCO3-則會被排出到尿中<這也就是metabolic alkalosis時體內尿中會排出多餘的HCO3-的原因。>
- PCO2:增加PCO2會造成增加HCO3-的吸收,由圖我們可以很清楚的看到因為PCO2增加會使得細胞中的H+增加,而造成H+secretion增加因而增加HCO3-的靜吸收。
- 有沒有覺得很熟悉,這也就是腎臟在respiratory acidosis時代償造成血中的HCO3-濃度上昇的代償原因,增加HCO3-在近曲小管的吸收。
而相對的,減少PCO2 and H+secretion decrease當然這個機轉也解釋了respiratory alkalosis時HCO3-濃度下降的原因。
當然臨床我們要另外記得記得
急性的respiratory acidosis recompensate時要乘以0.1,慢性時要乘以0.3的PaCO2改變。來判斷代償是否合理。
而respiratory alkalosis則是乘以0.2 and 0.4。
3. ECF volime: ECF volume expansion decreased HCO3- reabsorption.
ECF volume contractionàincreased HCO3- reabsorption
(有名的Contraction alkalosis)
- Angiotensin II:會刺激NA+-H+ exchange因此增加HCO3-吸收。contraction alkalosis occurs secondary to ECF volume contraction.
Excretion of fixed H+: 由蛋白質和磷脂質代謝而來的酸,由titratable acid and NH4+排出。
As Trtratable acid(H2PO4-):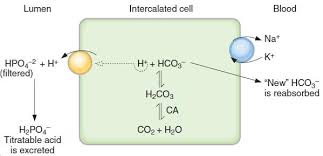
排出的多少由amount of urinary buffer and the pK of the buffer來決定。
由上圖可以看到H+ and HCO3-產生後,HCO3-直接吸收入血液,而H+則藉由H+-ATPase排出,排出的H+和filter過的HPO42-結合而產生titratable acid H2PO4-
這裡面要注意的是H+-ATPase受到aldosterone的影響而增加。
還有這個過程造成的是 H+的淨分泌還有HCO3-的淨吸收。
因為H+secretion 所以 pH of urine的下降,但尿液pH最低只可到達4.4
As NH4+:

決定H+的排出的關鍵在於NH3在腎細胞的合成數量以及urine pH!
NH3在腎細胞由glutamine產生,產生後會擴散到lumen from the cells.
HCO3- 一樣造成一個淨吸收,而H+ 則也是藉由H+ATPase secretion 到lumen side和NH3àNH4+,而排出。(稱為diffusion trapping)
Lumen side pH越低造成越多的NH4+ secretion出,同時在low pH時lumen side NH4+數量>NH3越多因此也造成NH3的diffusion gradient 增加。
另外重要的是NH3製造的影響因子:
1.在Acidosis時會增加 NH3的製造這也幫助了H+ 的排出
2.高血鉀則會抑制NH3的合成,因此減少H3的排出(type IV RTA 的機轉。)
3.低血鉀則會刺激NH3的合成而增加H+的排出。
到這邊基本上把腎臟調節酸鹼的基礎都簡單複習過了~
接下來就進入Metabolic acidosis啦!
- 一般是由過度的產生或攝入fixed acid or loss of base produces 動脈中的H+增加(acidemia)
- HCO3-這時就被當成緩衝液for extra fixed acid.-->arterial HCO3- decrease.
- Acidemia 同時會造成hyperventilation(Kussmaul breathing )因為respiratory compensation for metabolic acidosis.
- 體內的酸增加腎臟會開始排出多餘的H+ as titratable acid and NH4+ and increased resorption of HCO3-àreplenished the HCO3- used in buffering the added fixed H+.
- 在慢性的metabolic acidosis, adaptive increase NH3 synthesis才另外增加幫助酸的排除!
Serum anion gap=<Na>-<Cl+HCO3->=unmeasured anions-unmeasured cations
Unmeasured anion includes: phosphate,citrate,sulfate,and protein
Normal value is 12mEq/L(rage:8-16mEq/L)
在代謝性酸中毒中,HCO3-被當成緩衝液而滴定掉了,這時會注意到公式的左側HCO3- decreased這時為了要符合電中性原則,
勢必要有另外的陰離子變高,這也就是Anion gap的原理,另外的陰離子可以是Cl-也可以是other unmeasured anion.
因此:
The serum anion gap is increased如果此增加的陰離子是unmeasured anion(ex.phosphate,lactate,beta-hydroxybutyrate, and formate)is increased to replace HCO3-
The serum anion gap is normal 如果增加的陰離子是Cl-造成hyperchloremic metabolic acidosis.
所以我們算Anion gap出是High anion gap metabolic acidosis 就會知道左側公式是HCO3- decrease=右側公式unmeasured anion increased
而算出normal anion gap 就會知道左側公式的HCO3-decreased=Cl increase所以整體gap不增不減!
至於當high anion gap時需要再算的 delta delta anion gap
delta detal AG= delta AG / delta HCO3-
一般來說 1-2都算正常,就顯而易見的是要看看是否HCO3-的改變和unmeasured anion的改變是否成比例,如果沒有代表體內還有額外的其他事情發生!例如另外的代謝鹼。
至於為啥只有在metabolic acidosis時可以算AG-->小編認為是只有在metabolic acidosis時才比較會有unmeasured anion or cation出現和
類似buffer的狀況產生,而造成HCO3-被滴定掉的量等於新產生的fixed acid的量。
希望有幫助到各位!


 留言列表
留言列表


